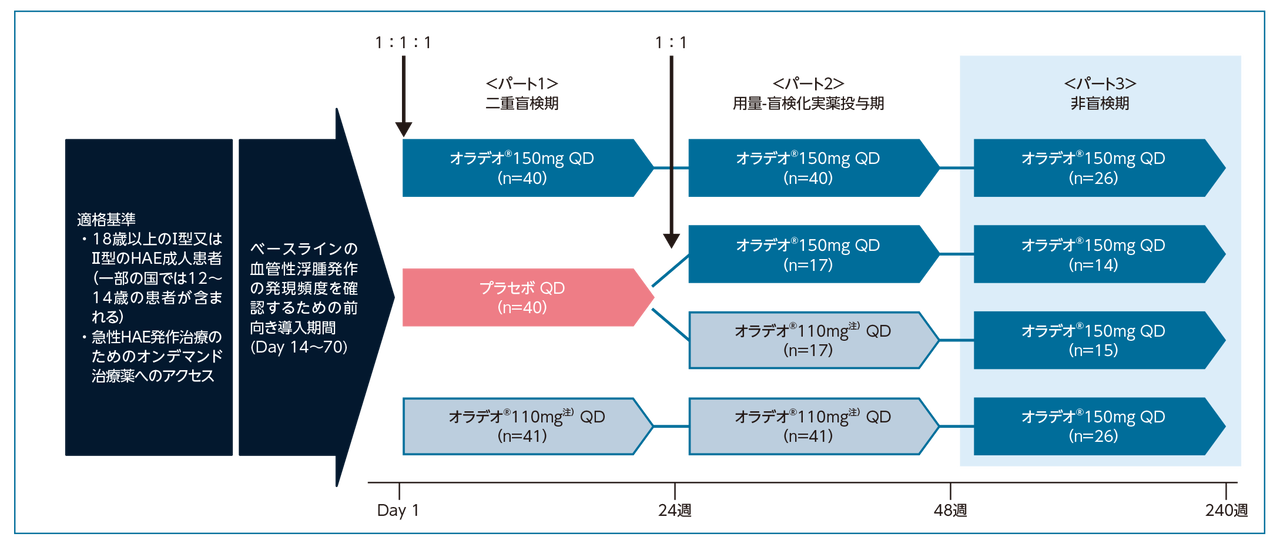
APeX-2試験全体で最も多く報告されたTEAEaは、上気道感染b、腹痛及び下痢であった1),2) 。
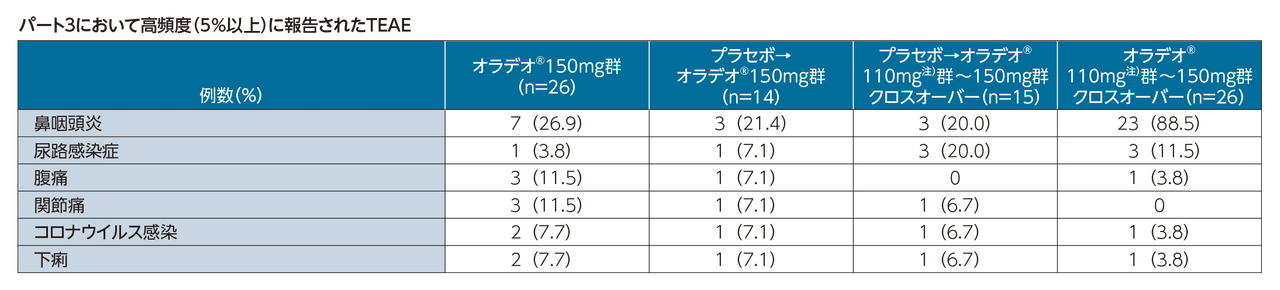
a 高頻度のTEAEは、APeX-2のパート1、パート2、パート3でそれぞれいずれかの治療群で10%以上、いずれかのオラデオ®群の10%以上、集団全体の5%以上に発生したものと定義した1),2) 。
b「上気道感染」は、基本語の鼻咽頭炎、上気道感染およびウイルス性上気道感染を含む。
1)Zuraw, et al. J Allergy Clin Immunol. 2021, 148(1): 164-172
2)Wedner HJ, et al. J Allergy Clin Immunol Pract. 2021, 9: 2305-14
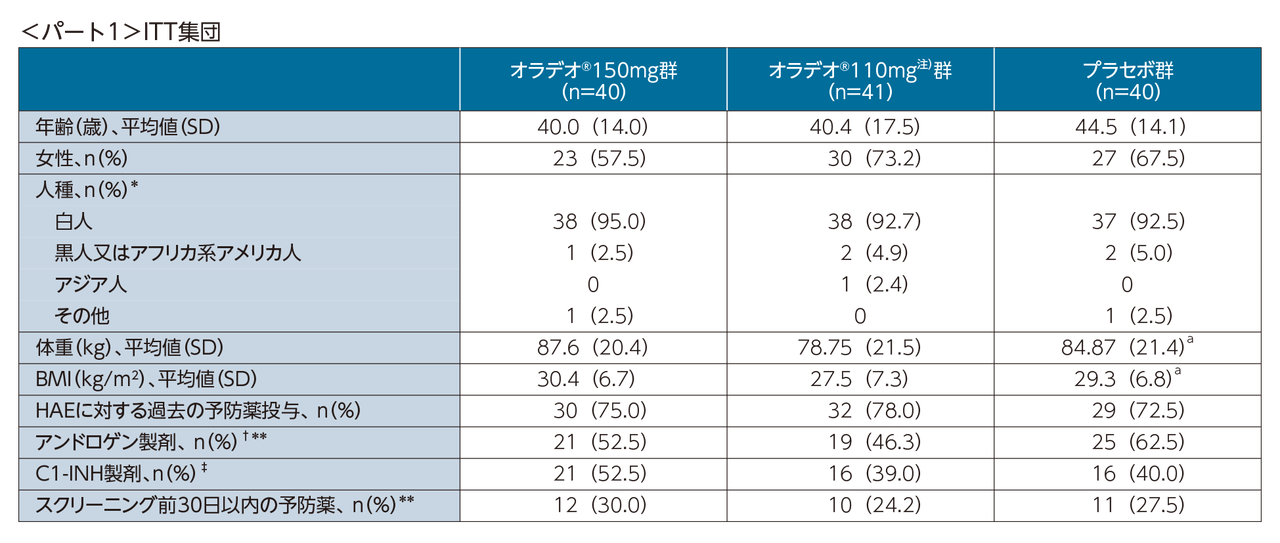
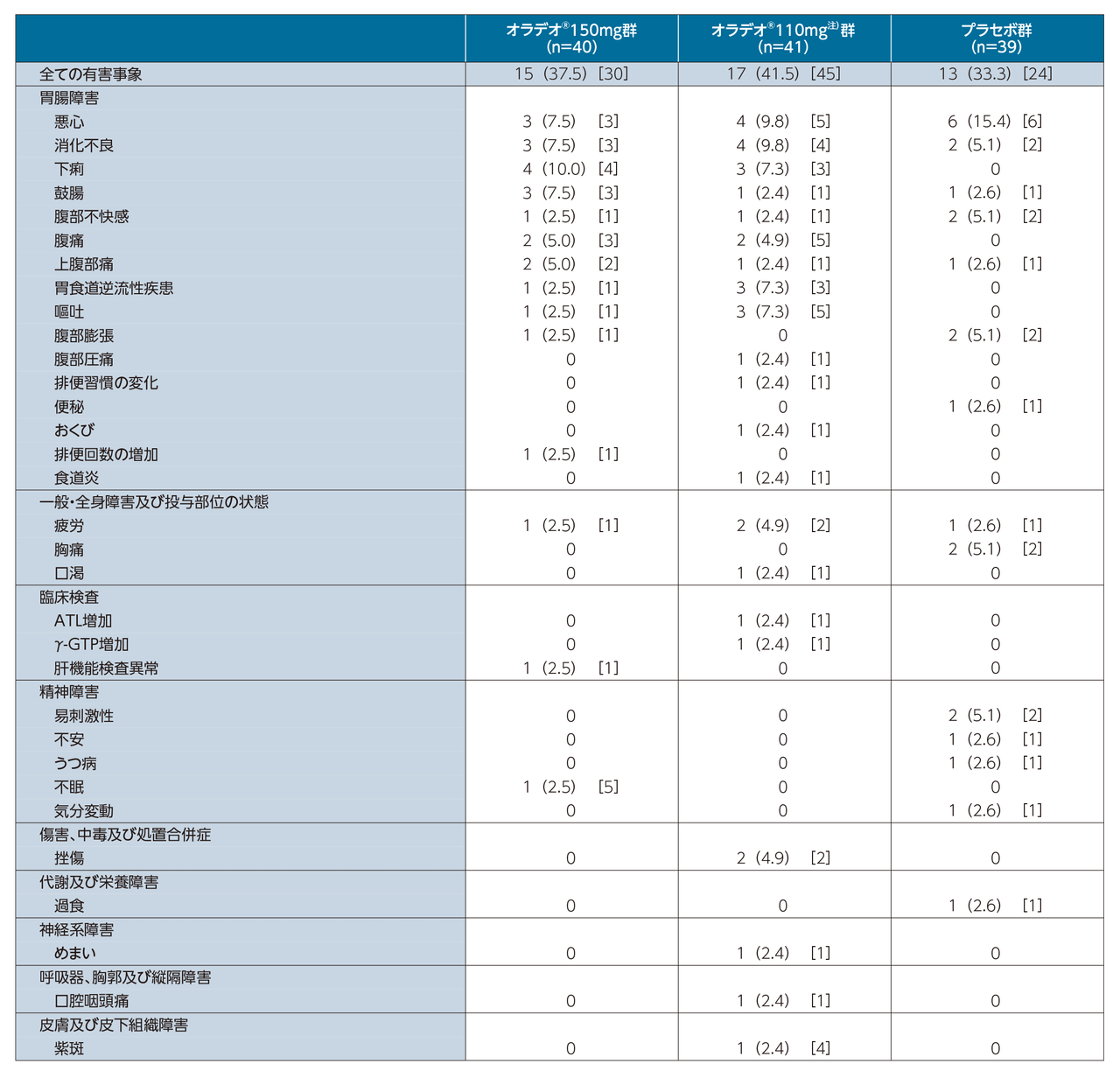
パート1における有害事象の発現状況
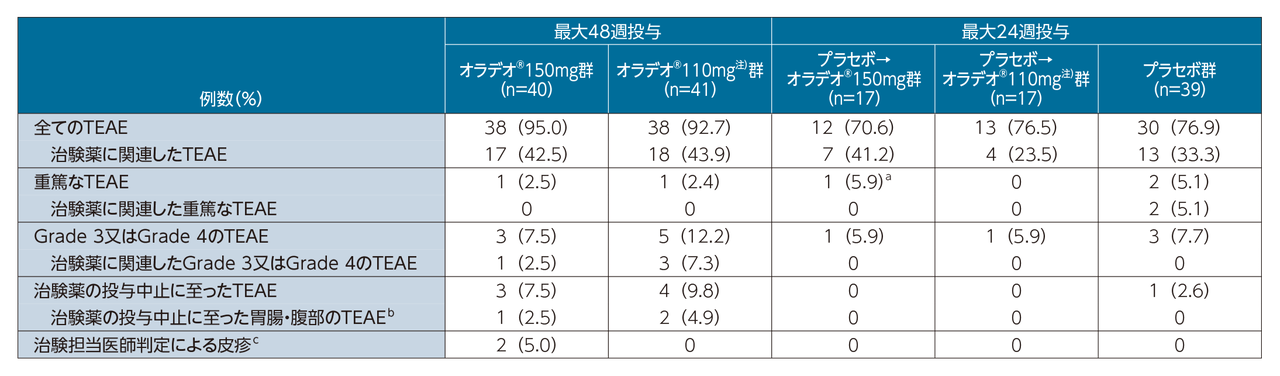
有害事象は、オラデオ®150mg群で15/40例(37.5%)、オラデオ® 110mg注)群で17/41例(41.5%)、プラセボ群で13/39例(33.3%)に認められた。投与中止に至った有害事象は、オラデオ® 150mg群で肝機能検査値異常1例、オラデオ® 110mg注)群で悪心、消化不良、嘔吐1例並びに紫斑1例、プラセボ群でうつ病1例が認められた。重篤な有害事象及び死亡例は各群とも認められなかった。
主な有害事象は、オラデオ® 150mg群で下痢4例(10.0%)、悪心、消化不良及び鼓腸各3例(7.5%)など、オラデオ® 110mg注)群で悪心及び消化不良各4 例(9.8%)、下痢、胃食道逆流性疾患及び嘔吐各3例(7.3%)など、プラセボ群で悪心6例(15.4%)などであった。
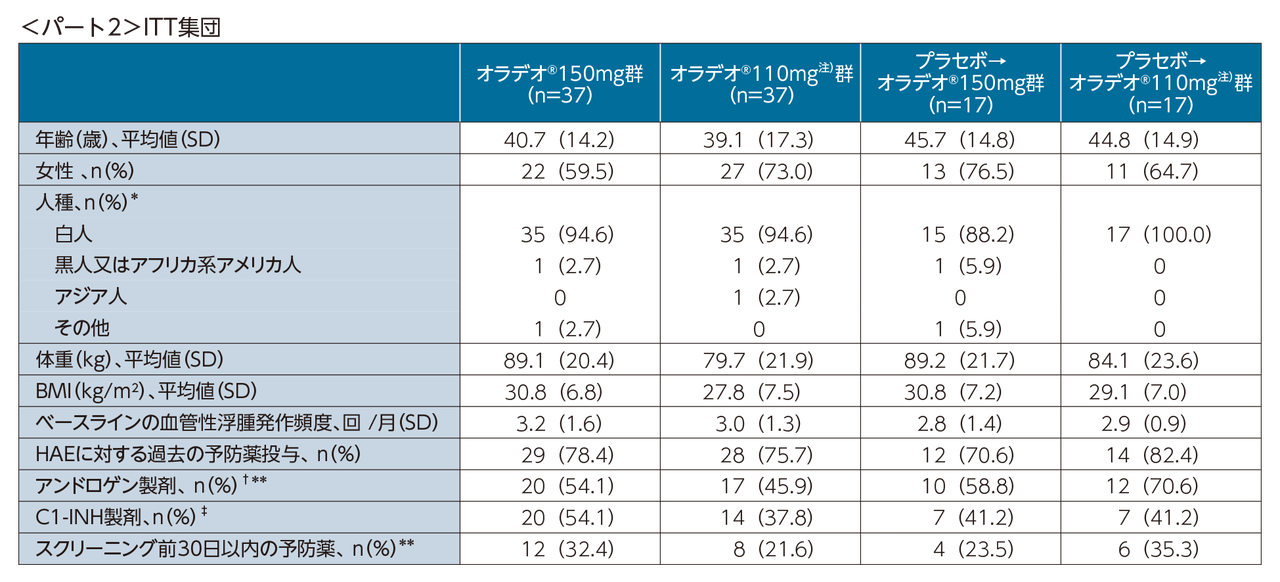
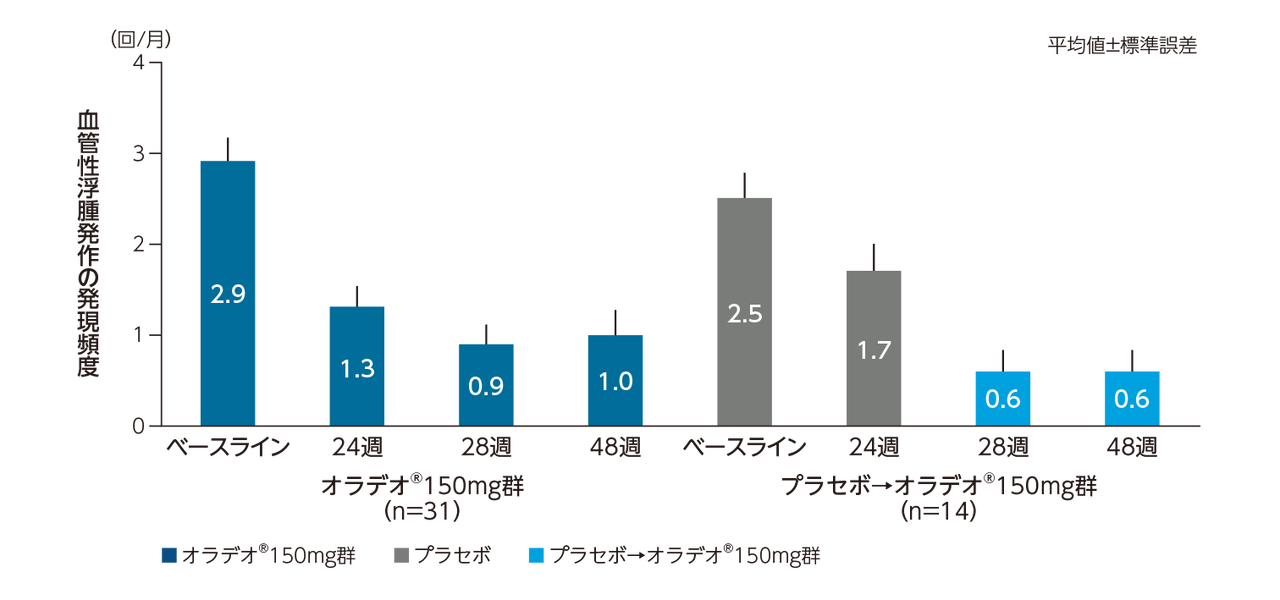
パート2におけるTEAEの概要(安全性解析対象集団)
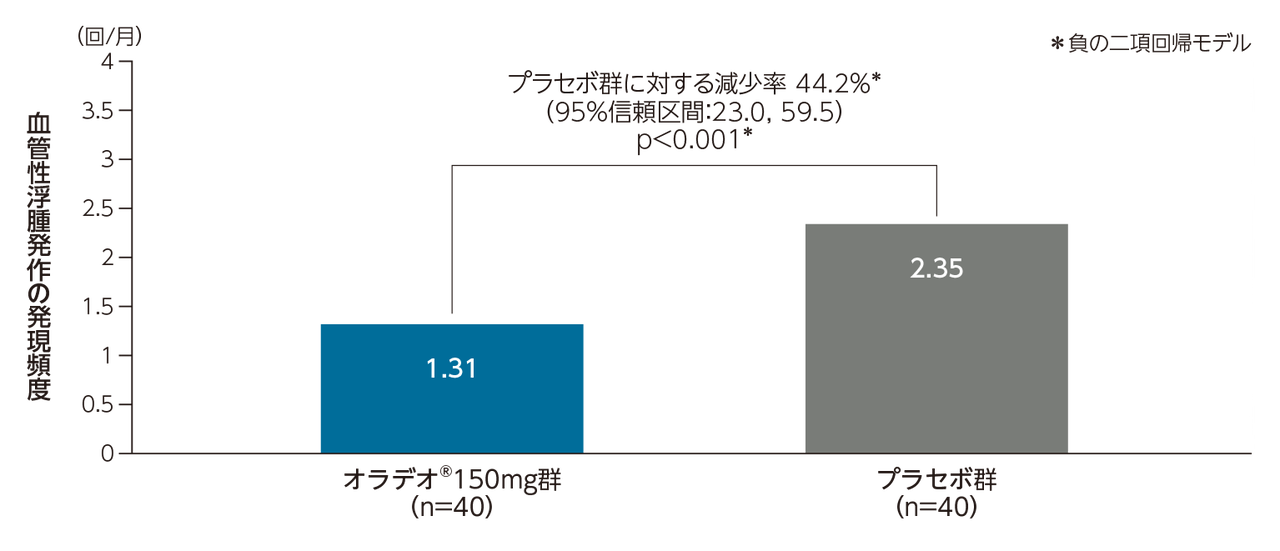
[APeX-2試験パート2 主要評価項目]
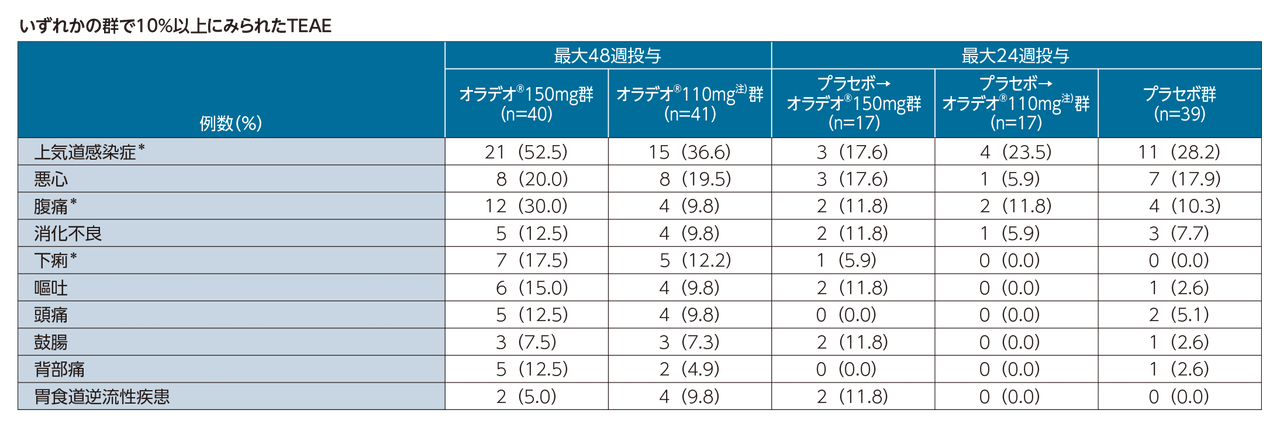
有害事象のほとんどは軽度または中等度であった。最も頻度の高い有害事象(パート1又はパート2のいずれかの治療群において患者の10%以上に報告されたもの)は、上気道感染症、悪心、腹痛、消化不良、下痢、嘔吐、頭痛、鼓腸、胃食道逆流症、背部痛であった。
すべての原因によるグレード3または4のTEAEは、パート1および2でオラデオ®群に無作為化された81名の患者のうち8名(10%)、パート1でプラセボ群に無作為化された39名の患者のうち3名(8%)、およびパート2でプラセボ群からオラデオ®群へ再無作為化された34名の患者のうち2名(6%)で報告された。薬物関連のグレード4の有害事象は報告されなかった。
* 「上気道感染症」、「腹痛」、「下痢」には複数の基本語(PT)が含まれる。「上気道感染症」には「鼻咽頭炎」、「上気道感染症」及び「ウイルス性上気道感染症」のPTが含まれる。
「腹痛」には、「腹痛」、「腹部不快感」、「上腹部痛」、「腹部圧痛」のPTが含まれる。「下痢」には、「下痢」及び「頻繁な排便」のPTが含まれる。
a 子宮筋腫:パート1のプラセボ群で認められた。
b 治験中止に至った胃腸・腹部のTEAE:MedDRA v19.1の高位グループ語(HLGT)である。(1)胃腸兆候及び症状又は(2)排便障害に含まれる基本語(PT)に該当するすべての有害事象である。
c 治験担当医師判定による皮疹:治験医師が有害事象例報告書で特に関心のある有害事象として記載した有害事象。
TEAEは治験薬投与開始後48週までの(被験者が48週前に中止した場合は最終投与後30日以内の)有害事象と定義。
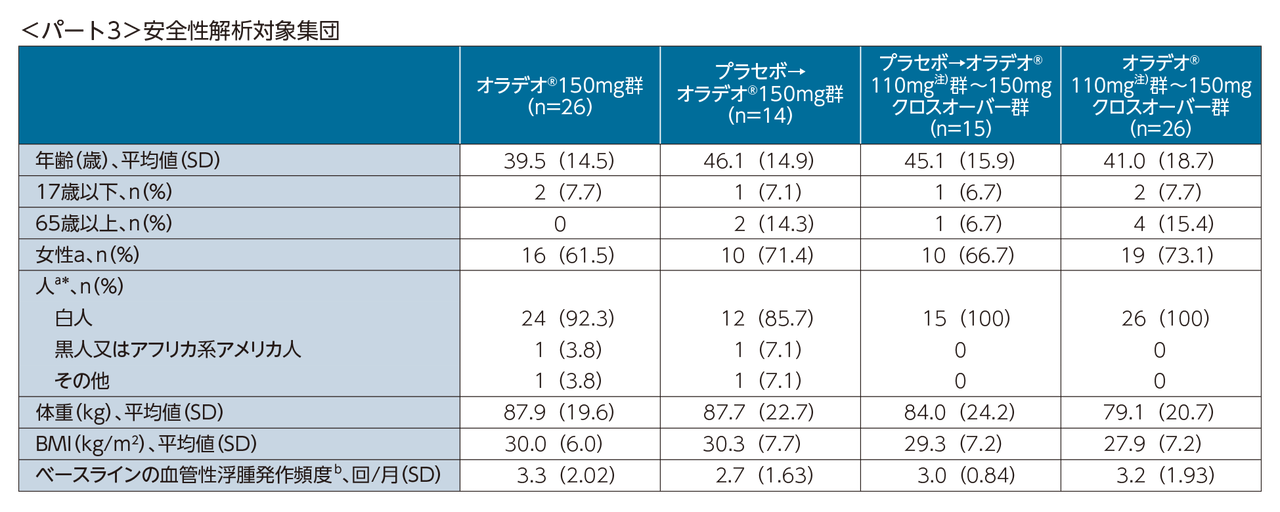
パート3におけるTEAEの概要(安全性解析対象集団)
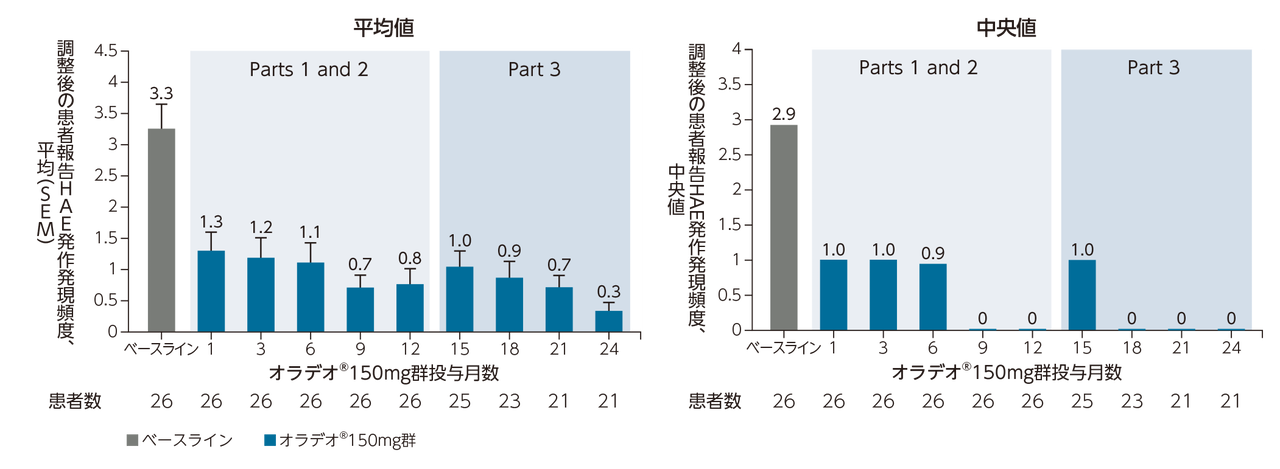
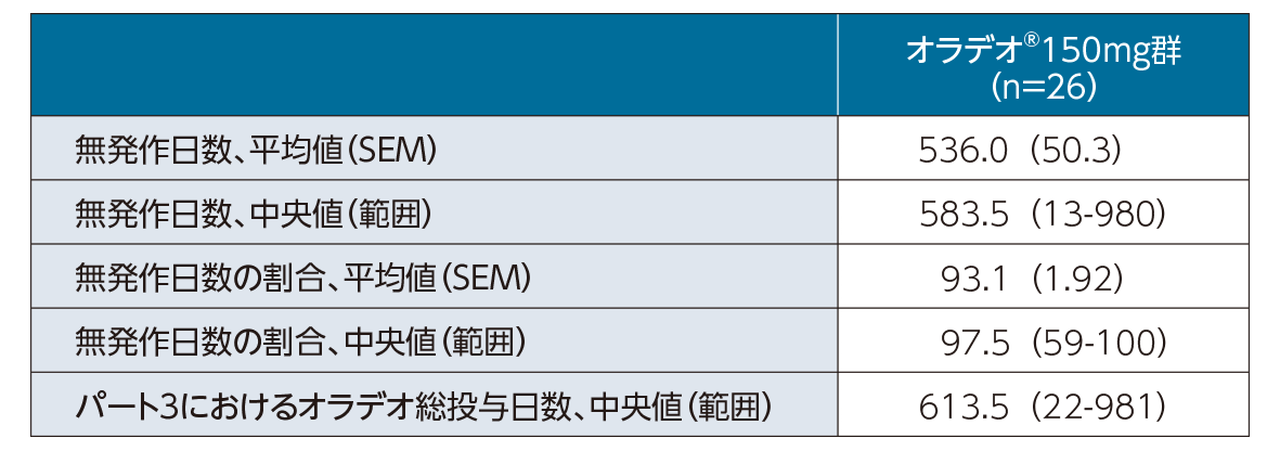
[APeX-2試験パート3 主要評価項目]
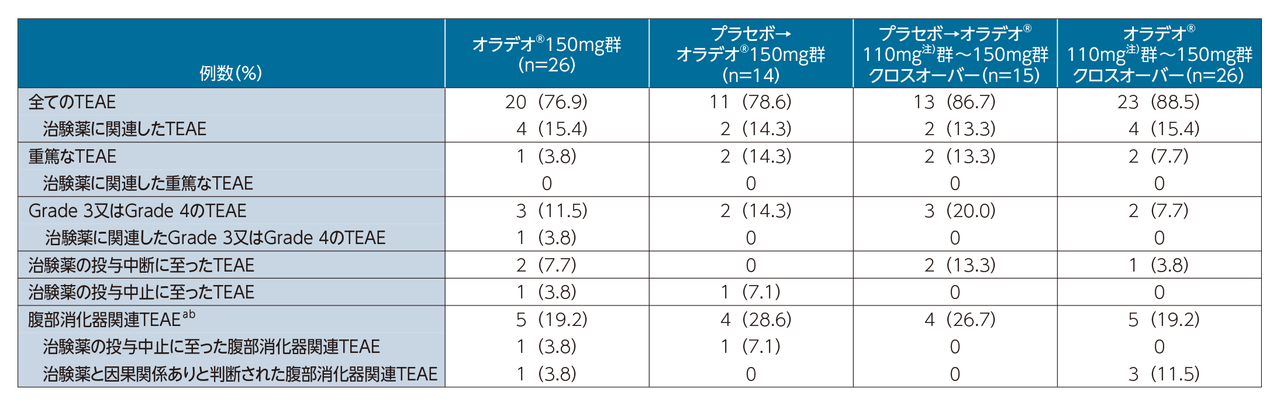
APeX試験パート3の結果は、全体としてパート1および2で報告された安全性および有効性の結果と一致している。
パート3では、81例全例がオラデオ®150mgを投与され中央値(範囲)644(22-981)日間治療を受けた。この期間中、新たな安全性シグナルは認められず、ほとんどのTEAEは軽度または中等度であり、治験薬と関連のあるTESAEは報告されなかった。
治験薬と関連のある腹部消化器系TEAEの割合は、パート1とパート2の患者(40.7%)と比較してパート3では大幅に少なかったことから(4.9%)、治療早期に発現したというこれまでの報告を裏付けるものである。
 HOME
HOME