24週間の投与期間における専門医判定による血管性浮腫発作の発現頻度
[APeX-J試験パート1 主要評価項目]
専門医判定による血管性浮腫発作の発現頻度は、オラデオ®150mg群で1.11回/月であり、プラセボ群の2.18回/月に対する減少率は、49.1%(95%CI:20.4, 67.5、p=0.003、負の二項回帰モデル※)と有意な減少が認められた。
 HOME
> オラデオ®の臨床試験 >
国内第Ⅲ相試験APeX-J試験[国内データ]
HOME
> オラデオ®の臨床試験 >
国内第Ⅲ相試験APeX-J試験[国内データ]
Ohsawa I, et al. Allergy 2021, 76 (6): 1789-1799
社内資料(国内第Ⅲ相試験:301試験)(2021年1月承認、CTD 2.7.6.15)[承認時評価資料]
Honda D, et al. World Allergy Organ J. 2024, 17(3):100882. doi: 10.1016/j.waojou.2024. 100882
本試験には一部承認外の用法及び用量が含まれますが、用量設定を目的のひとつとした試験であり、かつPart 1は承認時評価資料であるため、副作用発現状況のデータについては掲載し、その他のデータについては承認の範囲内の用法及び用量の症例群に限定し、一部改変して掲載しています。
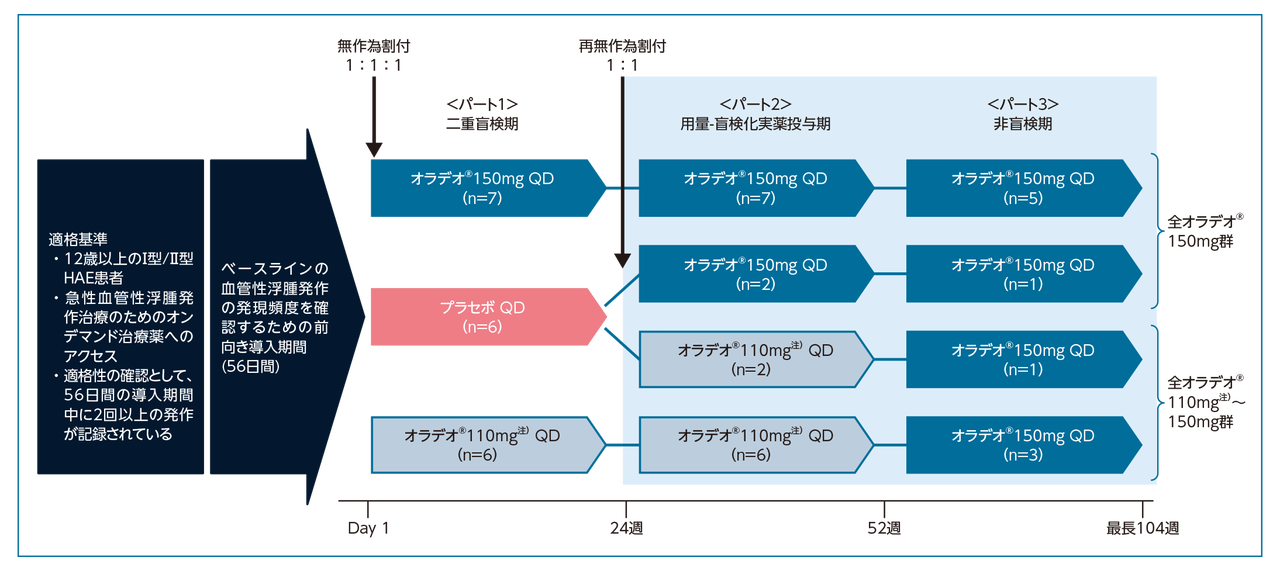
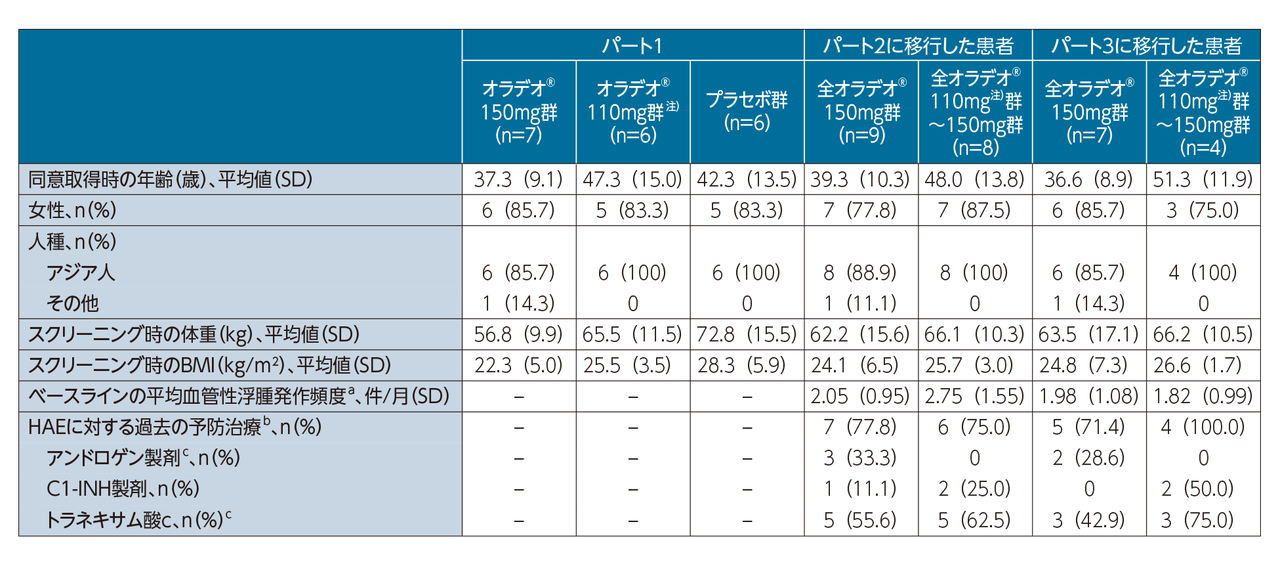
試験概要
臨床効果
専門医判定による血管性浮腫発作の発現頻度は、オラデオ®150mg群で1.11回/月であり、プラセボ群の2.18回/月に対する減少率は、49.1%(95%CI:20.4, 67.5、p=0.003、負の二項回帰モデル※)と有意な減少が認められた。

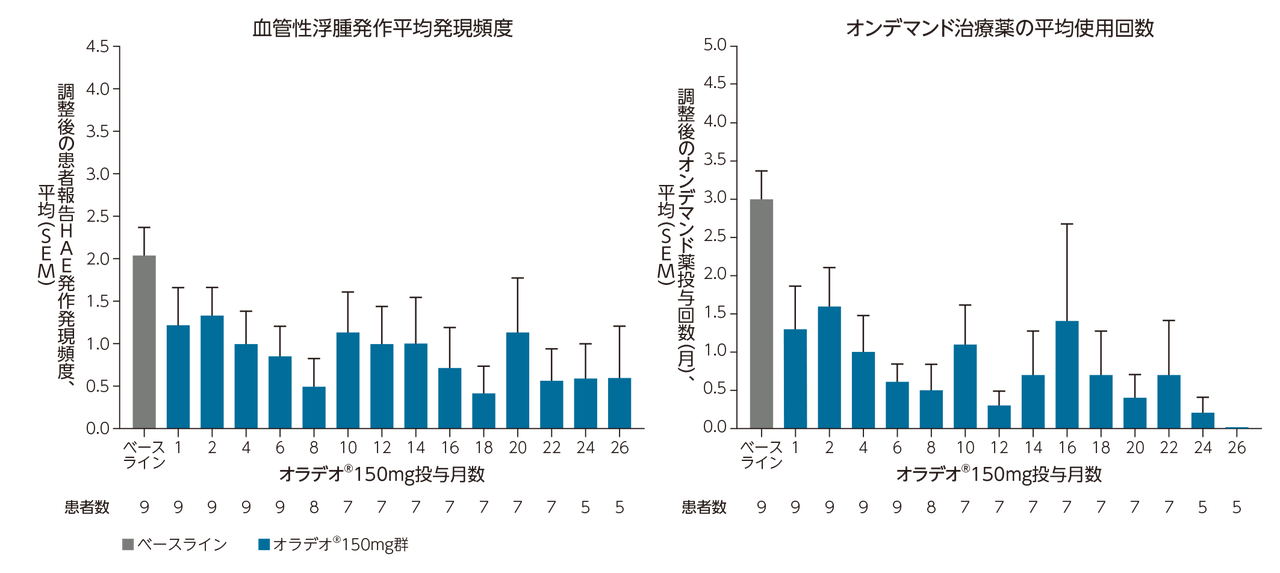
HAE発作発現頻度は、投与後1ヵ月から低下傾向が認められ、全150mg群の投与26ヵ月目における発作発現頻度の中央値は0回であった。また、投与26ヵ月目における1ヵ月あたりの平均オンデマンド治療薬の使用回数は0.0(0.0)回であった。
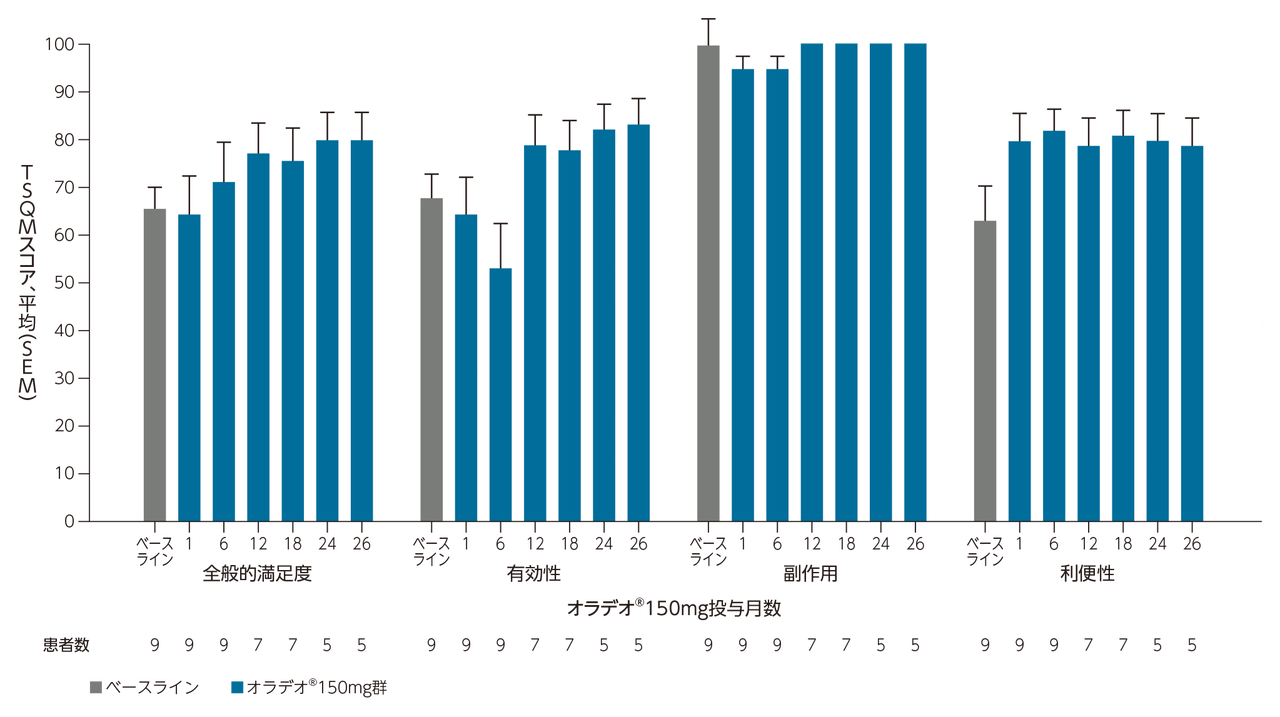
26ヵ月間の試験期間中、オラデオ®投与により、有効性、利便性ならびに全般的満足度スコアに改善傾向が認められた。
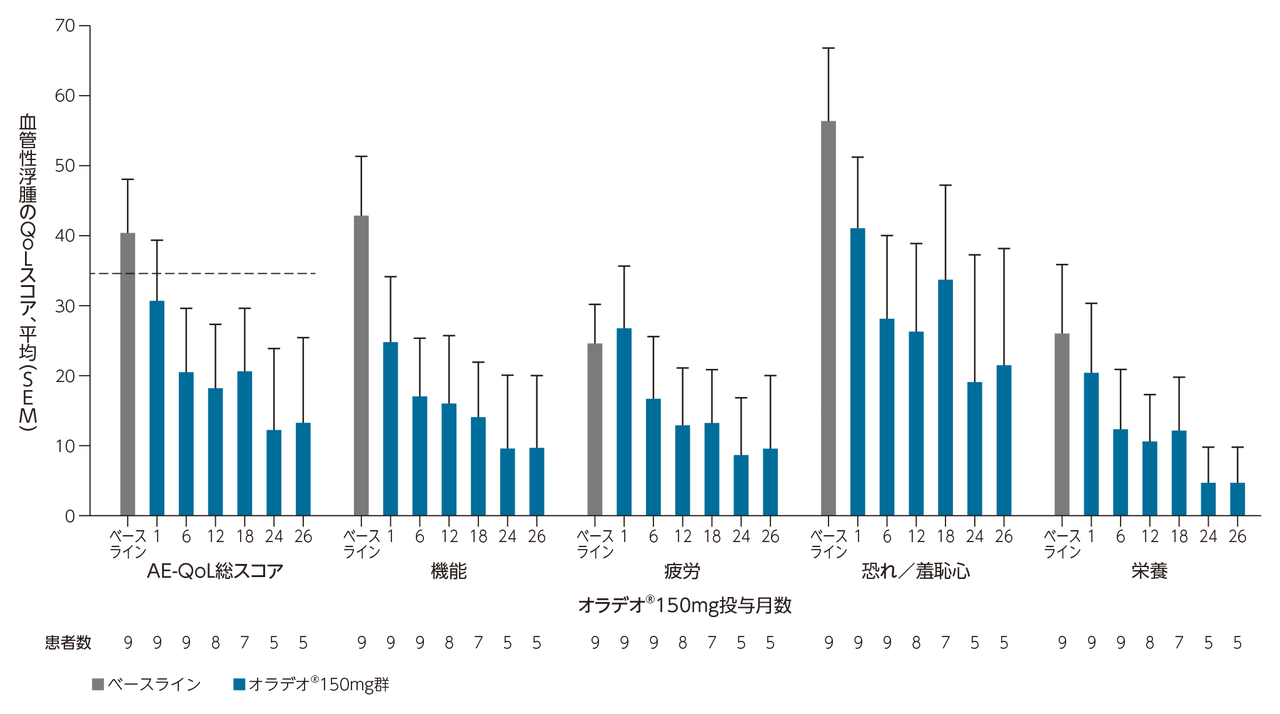
オラデオ®投与後、QOLの指標であるAE-QoLの各ドメインスコアで改善が認められ、AE-QoL総スコアの改善はMCIDを上回った*。
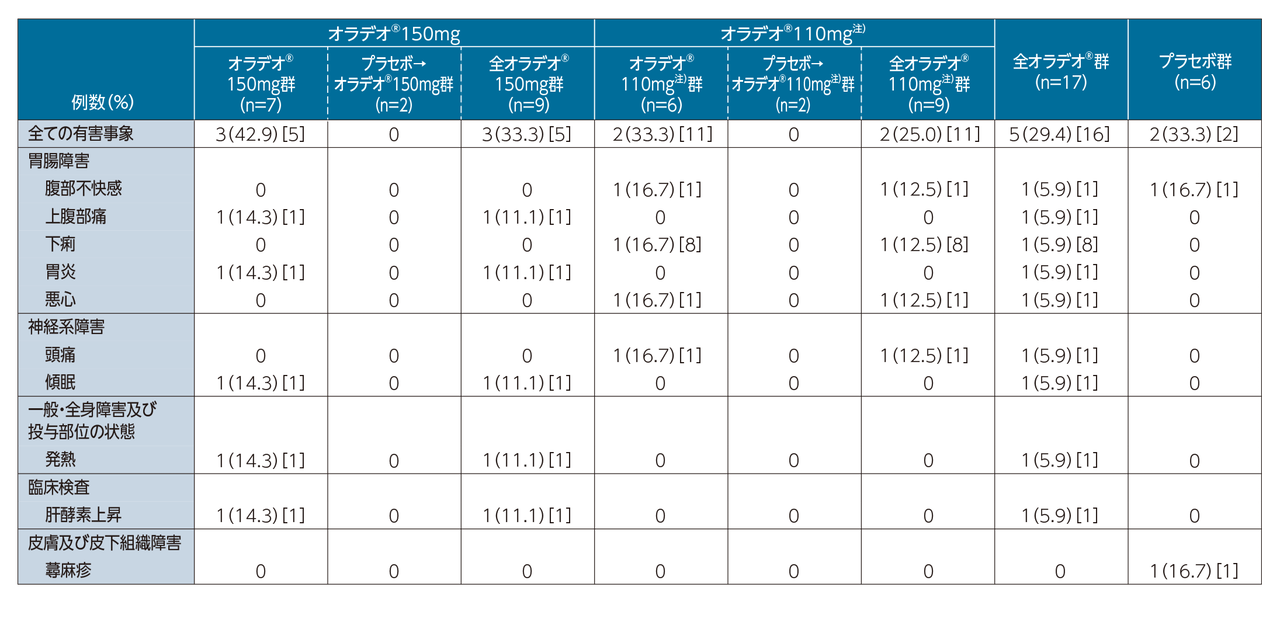
安全性
本試験における有害事象は、オラデオ®150mg群全体で3/9例(33.3%)、オラデオ®110mg注)群全体で2/8例(25.0%)、 プラセボ群で2/6例(33.3%)に認められた。投与中止に至った有害事象は、オラデオ®150mg群全体で肝酵素上昇が1例、 プラセボ群で蕁麻疹が1例に認められ、オラデオ®110mg注)群全体では認められなかった。 重篤な有害事象及び死亡例は各群とも認められなかった。各群の有害事象の内訳は、オラデオ®150mg群全体で上腹部痛、 胃炎、傾眠、発熱、肝酵素上昇各1例(11.1%)、オラデオ®110mg注)群全体で腹部不快感、下痢、悪心、頭痛各1例 (12.5%)、プラセボ群で腹部不快感、蕁麻疹各1例(16.7%)であった。
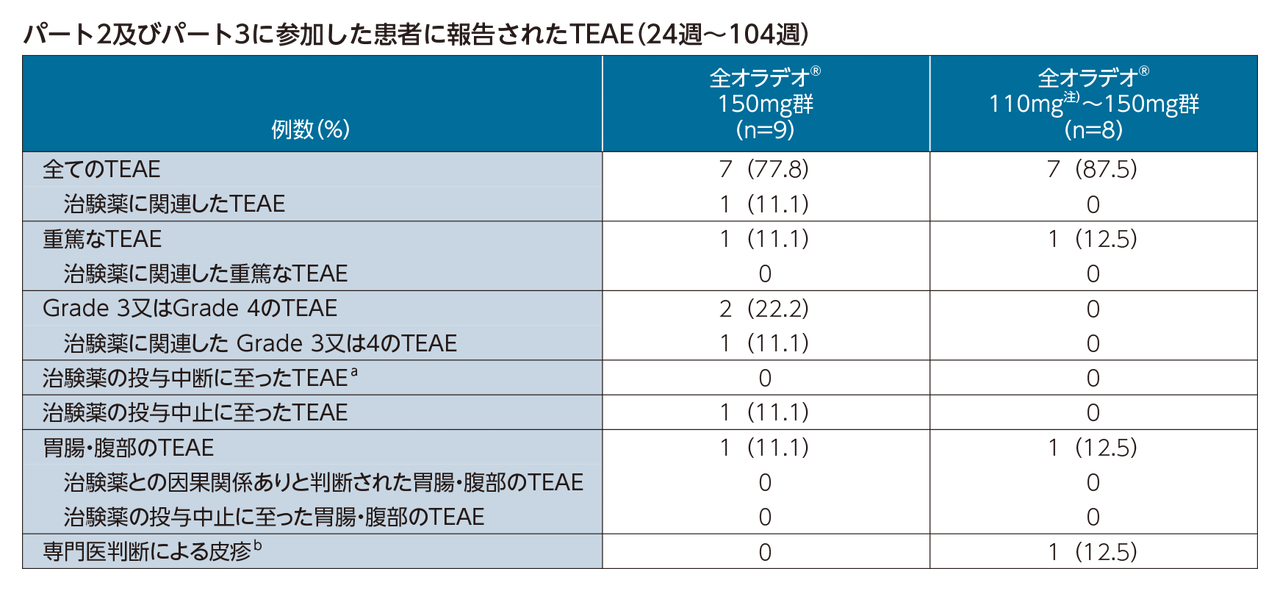
パート2及びパート3に参加した患者のオラデオ曝露期間の中央値(範囲)は554(77~650)日であった。パート2及びパート3の期間中、14例(82.4%)でTEAEを発現した。ほとんどのTEAEの重症度は軽度又は中等度であり、治験薬と関連のある重篤なTEAEは報告されなかった。
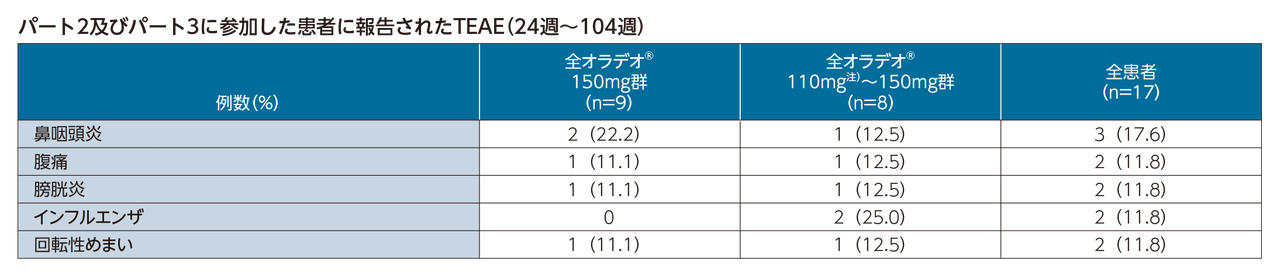
最も発現頻度の高いTEAEは、鼻咽頭炎、腹痛、膀胱炎、インフルエンザ、及び回転性めまいであった。