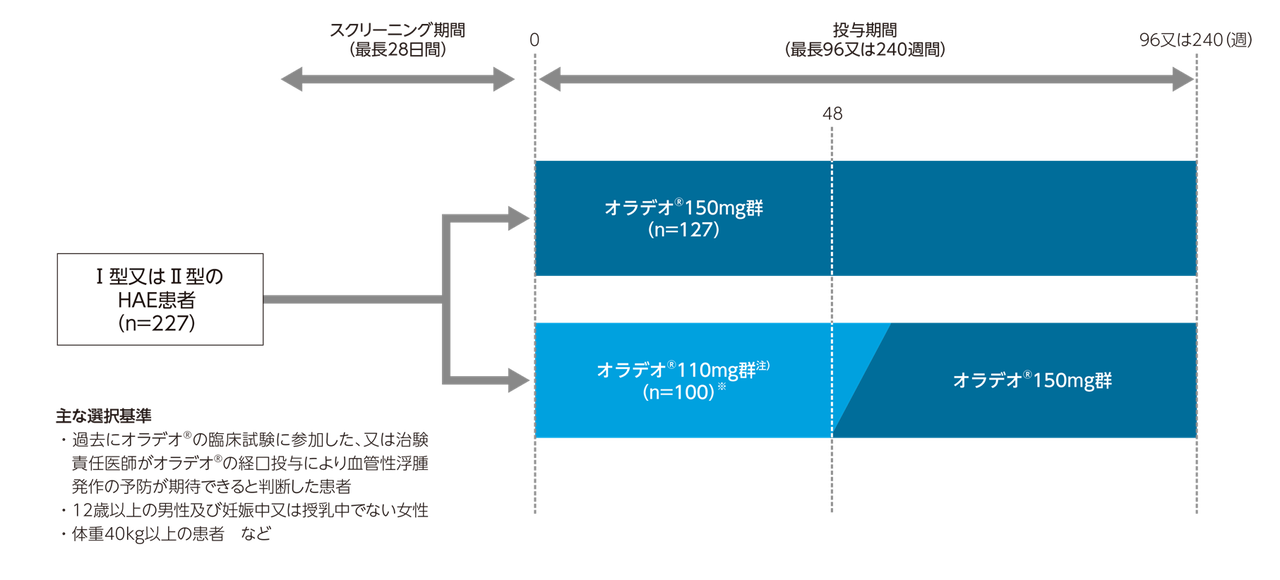
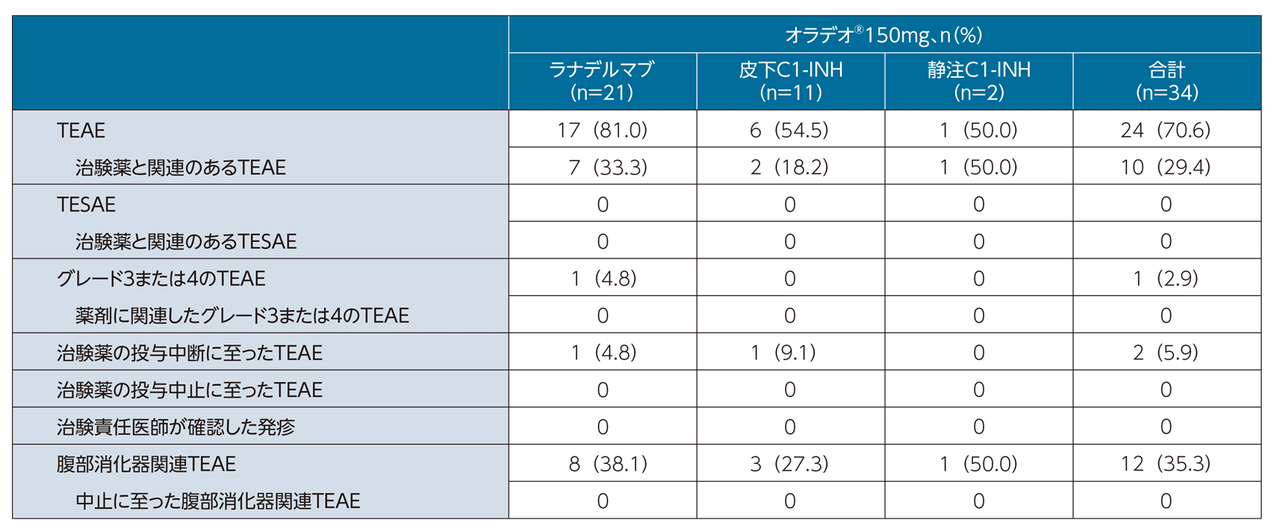
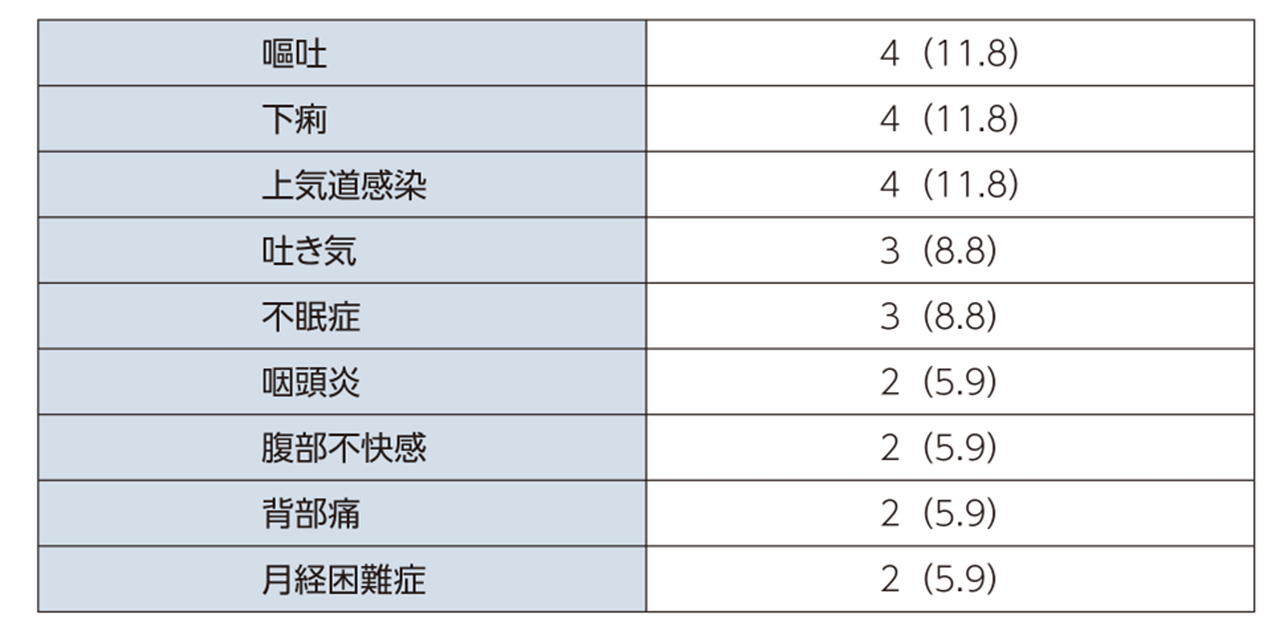
APeX-S試験には、一部承認外の用法・用量が含まれますが、承認時評価資料であるため、有害事象発現状況のデータについては掲載し、その他のデータについては承認の範囲内の150mg群に限定し、一部改変して掲載しています。
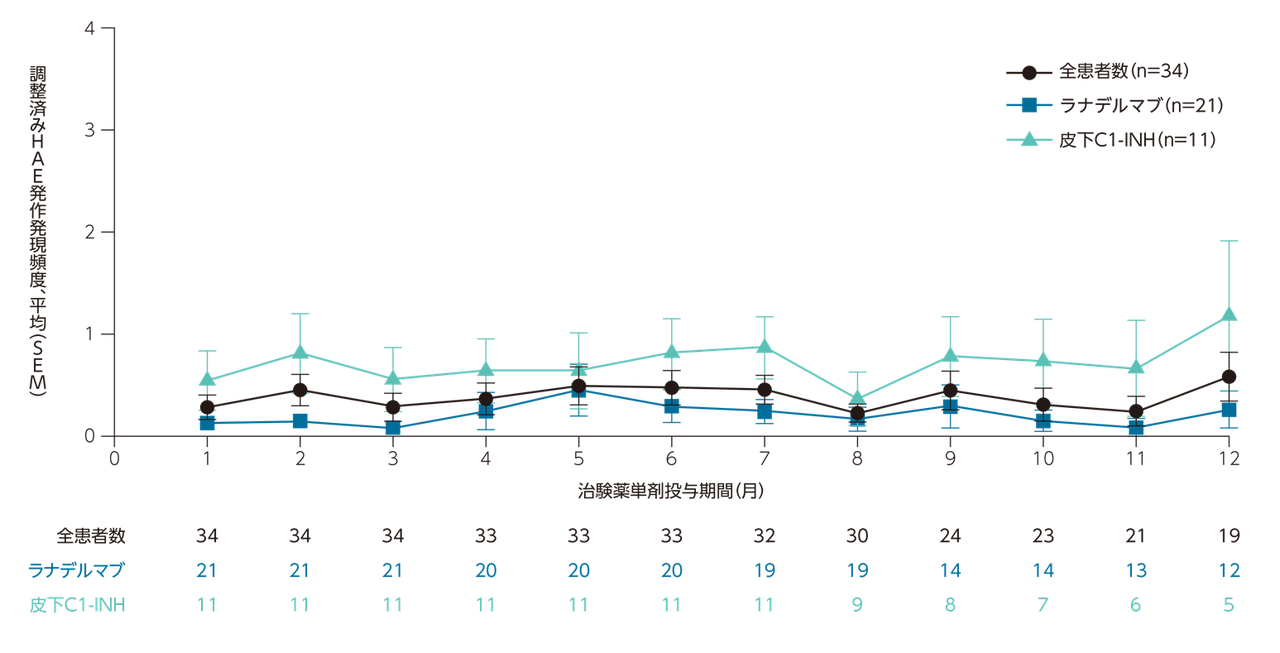
過去の長期予防薬から切り替えたオラデオ®単剤療法中の1ヵ月あたりの調整済み*HAE発作発現頻度
[副次評価項目]
*被験者が記録したすべての発作データを事前に定義された一連の基準に従って有効なデータか判定し、それを「調整済み」発作とした。
皮下注射C1-INHからオラデオ®単剤療法へ切り替えた患者では、発作頻度の平均(SD)は1ヵ月目で0.55 (0.28)、6ヵ月目で0.82(0.33)、12ヵ月目で1.18(0.72)であった。切り替え後のオラデオ®単剤療法の発作率の中央値は、12ヵ月間中9ヵ月において月0回を維持した。
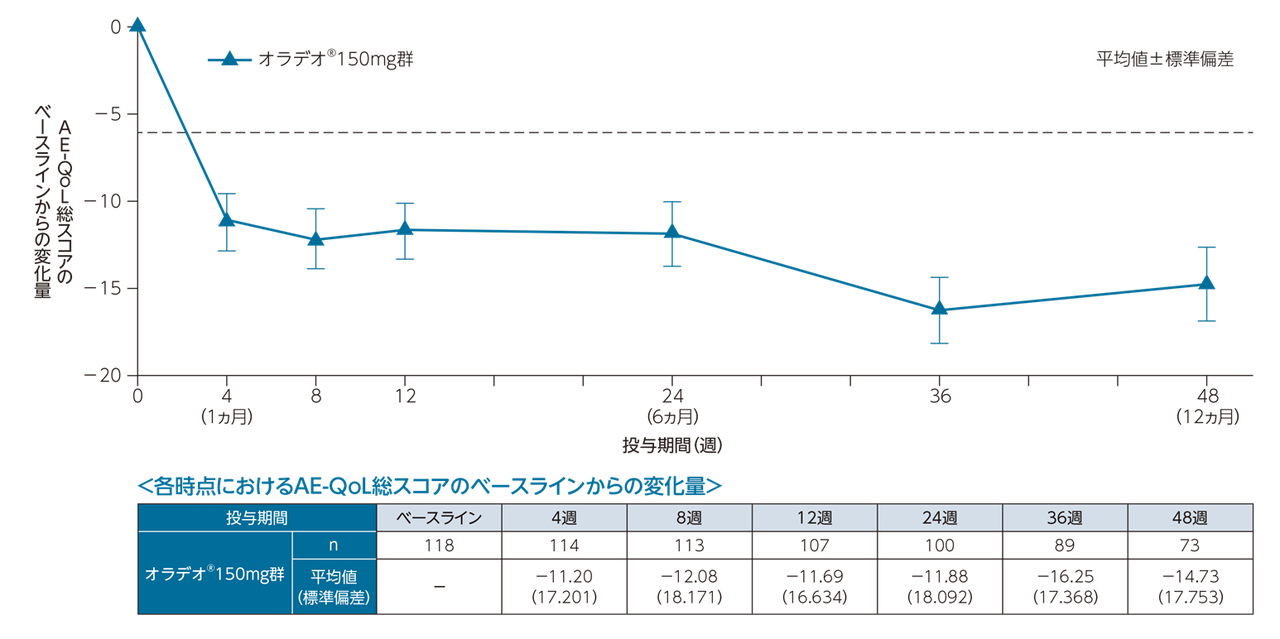
<参考情報> 48週間の投与期間におけるAE-QoL総スコアのベースラインからの変化量[副次評価項目]
ベースライン後初回評価(4週目)という早期段階で、MCID(臨床的意義のある最小差)である6点を上回る改善が認められた。
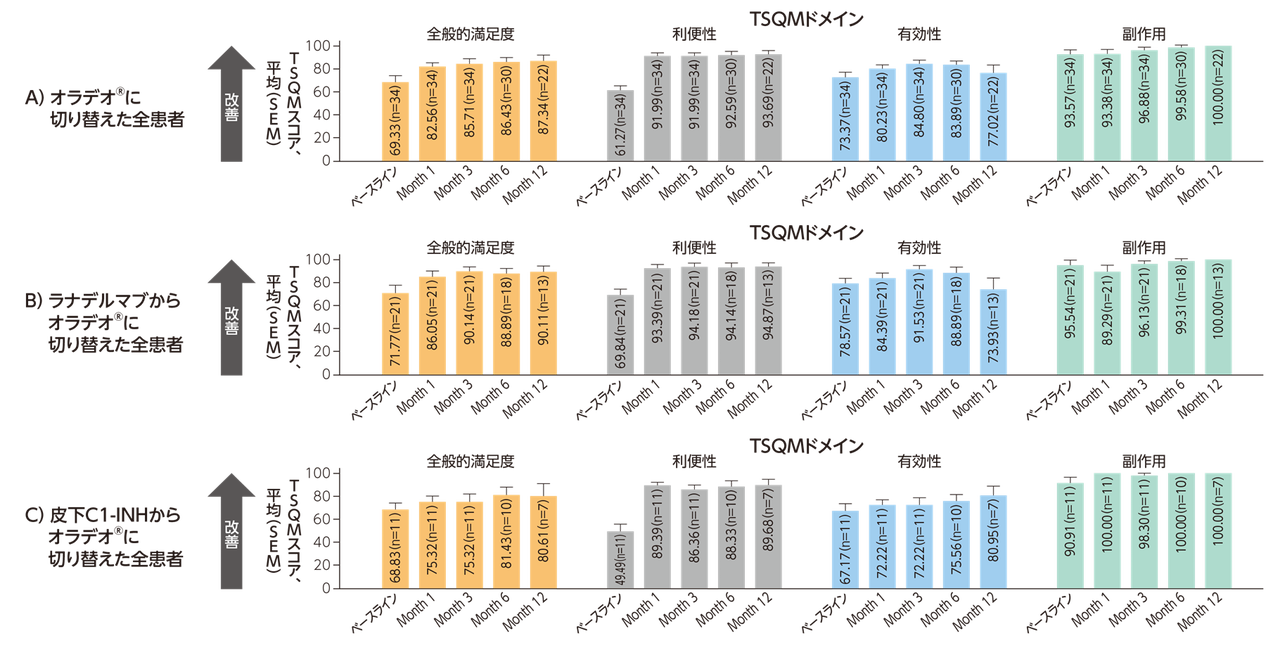
<参考情報>TSQMスケールスコア(平均SEM) [副次評価項目]
オラデオ®単剤療法に切り替えた全患者でTSQMスコアが改善し、ベースラインから12ヵ月目までの最大の変化が、利便性および全体的満足度で認められた。有効性と副作用スコアは、ベースラインから12ヵ月目までほぼ一貫していた(A)。
ラナデルマブからオラデオ®単剤療法へ切り替えた患者においてもTSQMスコアの改善傾向が認められ、ベースラインから12ヵ月目にかけて利便性および総合満足度は改善を示した(B)。
皮下注射C1-INHからオラデオ®に切り替えられた患者では、利便性、有効性、総合的満足度、有害事象において、ベースラインから12ヵ月目までの改善が認められた(C)。
 HOME
HOME